Vaccinatie geïnduceerd / injectieplaats sarcoom bij de kat
Gerard Rutteman (specialist veterinaire oncologie)
Inleiding
Eind jaren ’80, begin jaren ’90 werden voor het eerst vermoedens geuit over een mogelijke relatie tussen vaccineren en het ontstaan van fibrosarcomen (kwaadaardige tumoren van stug bindweefsel) bij de kat. (1) Enkele jaren later verscheen er een publicatie die nadrukkelijk een verband legde tussen vaccineren en het – bij de kat – ontwikkelen van fibrosarcomen op de injectieplaats (2)
Uit een grote studie (3) kwam naar voren dat het ontstaan van sarcomen op de injectieplaats gezien werd zonder verschil naar type vaccin of producent daarvan. Tevens had schudden, het mixen van verschillende vaccins, noch de wijze van toediening van de injectie enig verband met het ontstaan van sarcomen op de injectieplaats. Alleen gebruik van vaccin regelrecht uit de koelkast ging gepaard met het ontstaan van meer sarcomen dan wanneer het vaccin op kamertemperatuur was. Wat verder bij dit onderzoek naar voren kwam, was dat bepaalde lang-werkende injecteerbare medicijnen (zoals lang-werkende penicilline) mogelijk óók het ontstaan van sarcomen bij de kat doen toenemen.
De laatste jaren wordt vaker gesproken over “injection-site sarcoma” in plaats van vaccinatie geïnduceerd sarcoom. Overigens is het plaatsen van onderhuidse microchips vooralsnog niet aangewezen als risicofactor voor het optreden van een dergelijk sarcoom (4). Het meest evident als risicofactor is het gebruik van vaccins met adjuvans (‘versterker’). En daarbij gaat het vooral om vaccins tegen rabies en tegen feline leukemie virus (FeLV) (5).
Qua type is het meest voorkomende injectieplaats sarcoom het fibrosarcoom, maar andere typen komen ook voor, zoals rhabdomyosarcomen (met uiterlijk van tumoreuze spiercellen), myxosarcomen (veel tussenstof), chondrosarcomen (kraakbeen), ongedifferentieerde sarcomen (‘niet te plaatsen’) en maligne fibreuse histiocytomen (mengeling van stug bindweefsel en tumoreuze onstekingscellen). Veelal is er in en rond de tumor een forse ontstekingsreactie (6). Histologisch kenmerken al deze sarcomen zich als een agressief groeiende tumor.
Van alle weke delen sarcomen bij de kat maken de injectieplaats-sarcomen rond driekwart uit. In enkele katten zien we andere fibrosarcomen – veelal op jongere leeftijd -, die in verband worden gebracht met een totaal andere risicofactor, namelijk het feline sarcoma virus. De restgroep (ruim 20% van het totaal) zijn fibrosarcomen die niet tot deze twee oorzaken zijn terug te voeren.
Ziektekundige achtergrond (pathogenese)
De exacte pathogenese van injectieplaats sarcomen bij de kat is onbekend, maar locale irritatie en ontsteking lijken het optreden in aanzienlijke mate te bevorderen. Hierbij zou de vorming van zuurstof-radicalen, die vrijkomen in het verloop van een ontstekingsreactie, de tumorontwikkeling kunnen stimuleren (7). Tevens gaat een dergelijke ontstekingsactiviteit gepaard met hogere delingsactiviteit, die een beperkte vergroting van de kans op DNA-mutaties met zich meebrengt. De tijd tussen de injectie (vaccinatie / lang-werkend geneesmiddel) en het optreden van een injectieplaats wisselt van enkele maanden tot 10 jaar (3, 5, 8).
Bij vergelijking met andere zoogdieren, valt op dat dit hele fenomeen wel gerapporteerd is bij bepaalde muizen en nu dus de kat, maar geen rol van betekenis speelt bij hond of mens.
Mate van voorkomen, localisatie, diagnose
De mate van voorkomen (in technisch jargon: “incidentie”) van injectieplaats-sarcomen is circa 1-10 per 10.000 vaccinaties, alhoewel enkele auteurs zelfs een getal van 1 op 1000 vaccinaties noemen (5, 8). Voor Nederland is gebruik van rabies en FeLV vaccin niet frequent en wanneer ik voor de andere vaccins (zoals kattenziekte of panleukopenie) de laagste van de genoemde kansen hanteer, dan komen we hier te lande toch op enkele tientallen katten per jaar.
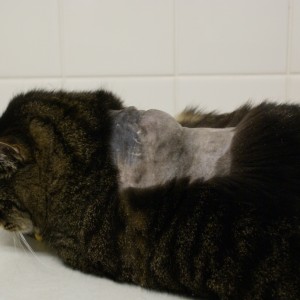
Fig. 1.: Kat met injectie-plaats sarcoom tussen de schouderbladen (courtesy Johannes Hirschberger)
Vaak worden deze sarcomen gezien aan de bovenzijde van de borst (thorax) aangetroffen, inclusief hals gebied tussen de schouderbladen (Fig 1.). Andere plaatsen zijn de flank, dij, lendenen of bilspier. Deze plaats hangt nauw samen met de praktijk van het geven van injecties: vroeger gebeurde dit vaak tussen de schouders.
Katten met een zwelling in/onder de huid op de plek waar in eerdere jaren injecties (incl. vaccins) zijn toegediend moeten verdacht worden van injectieplaats-sarcomen (5,8). De definitieve diagnose kan alleen worden gesteld weefselonderzoek. Daar deze tumoren kunnen uitzaaien (tot in plm 25%) is het van belang vooraf aan een eventuele behandeling röntgenfoto’s van de borstholte te maken.
De voornaamste oorzaak voor het optreden van hergroei (recidief) van het sarcoom volgend op een operatie, is het in eerste instantie niet volledig wegnemen van de tumor (5,8,9,10). Omdat deze tumoren zich in allerlei richtingen uitbreiden is het erg moeilijk ze volledig te verwijderen. Voor aanvang van de operatie moet de chirurg zoveel mogelijk informatie te hebben omtrent de uitgebreidheid van deze tumor. Gewone (natieve) röntgenfoto’s kunnen een beperkte inschatting geven van de grootte en uitgebreidheid van de tumor. Een CT-scan laat veel meer details laat zien van de grootte en uitgebreidheid en wordt derhalve aangeraden. Door gebruik van een contrastmiddel bij de CT-scan kunnen ook kleinere uitlopers van de tumor beter worden herkend, zodat op basis van het gehele beeld een beter chirurgisch plan kan worden gemaakt. Vaak kan voor de operatie de kans op succes worden berekend, en daarmee de noodzaak ook te bestralen als toeveging op de operatie. Een CT-scan ná operatie – bij verdenking op onvolledige verwijdering-, wordt gehinderd door de gevolgen van die operatie.
Therapie
Uit verschillende studies blijkt dat radicale chirurgische verwijdering met ruime marges de beste prognose geeft voor katten met een fibrosarcoom (9,10). Chemotherapie (misschien in beperkte mate) en bestralen (radiotherapie) lijken bij te dragen aan een langere ziektevrije periode of overlevingstijd (11,12,13).
De tumor dient inclusief en indien mogelijk met 3 of zelfs 5 cm omliggend weefsel te worden verwijderd. De tijd na eerste chirurgie tot lokaal recidief was aanmerkelijk langer voor katten geopereerd door chirurgen in meer gespecialiseerde klinieken dan in de eerste lijn (10).
In recente jaren is een medicijn ontwikkeld op basis van een virus (‘canary-pox virus’) dat gemanilupeerd is om een stof te produceren die de afweer stimuleert (interleukine-2, IL-2). Onder de naam Oncept (van Merial) is dit nu beschikbaar voor herhaalde injectie (5x) op de plek van een chirurgisch verwijderd injectieplaats sarcoom. De gehele behandeling is duur (alleen het produkt meer dan 3000 euro). Bijwerkingen waren gering. Bij toepassing bij katten na operatie en bestraling (!) gaf het een verdubbeling van het ziektevrije interval (14).
Prognose
Zoals eerder gemeld, voor de prognose is het van doorslaggevend belang of de randen van het verwijderde weefsel vrij zijn van tumorcellen. In katten waarbij een recidief tot ontwikkeling is gekomen is de prognose zeer gereserveerd, aangezien de resultaten van een tweede operatie een stuk slechter zijn.
Katten met wél complete verwijdering hebben significant langere tumor-vrije-periode (>16 versus 4 maanden) en overlevingstijd (>16 versus 9 maanden) dan katten met incomplete verwijdering. (9,10)
Preventie, vaccinatie-beleid
In Amerika houdt de “Vaccine-Associated Feline Sarcoma Task Force” zich bezig met het stimuleren van onderzoek en veranderen van vaccinatie-protocollen met als doel het verminderen van het risico op de vorming van sarcoma in katten.
Geadviseerd wordt om het moment en de locatie van vaccineren goed te documenteren. Enten tussen de schouderbladen is veelal het makkelijkst, maar een daar tot ontwikkeling komende tumor wordt vaak laat ontdekt, verborgen als ze zijn tussen de twee uitstekende scapulae. Door de genoemde taakgroep wordt geadviseerd het onderste gedeelte van de staart dan wel van een poot te gebruiken als locaties om vaccins toe te dienen (15). Uit chirurgisch oogpunt een begrijpelijk advies – voor als er een sarcoom ontstaat – maar praktisch bij veel katten lastig uitvoerbaar. Persoonlijk vind de schrijver vaccinatie ter hoogte van de bovenste helft van de 12 rib verkieslijk: een dikte wordt daar snel ontdekt, en radicale chirurgie is veelal mogelijk.
Een tweede advies van de “Vaccine-Assiociated Feline Sarcoma Task Force” luidt om de entplek regelmatig te kontroleren, en zwellingen die aanwezig zijn > 3 maanden later, met een afmeting > 2 cm, of die groei vertonen > 4 weken na de enting, chirurgisch te verwijderen.
Aanpassingen aan het vaccin (minder / geen adjuvans) hebben vooreerst nog geen duidelijke afname in de incidentie van injectie-plaats sarcoom teweeg gebracht (5)
Referenties
1.Hendrick MJ, Goldschmidt MH (1991) Do injection site reactions induce fibrosarcomas in cats? (lett). J Am Vet Med Assoc 199:968.
2.Kass PH, et al. (1993) Epidemiologic evidence for a causal relation between vaccination and fibrosarcoma tumorigenesis in cats. J Am Vet Med Assoc 203 (3):396-405
3.Kass PH, et al. (2003). Multicenter case-control study of risk factors associated with development of vaccine-associated sarcomas in cats. J Am Vet Med Assoc 223: 1283-1292.
4.Daly MK, et al. (2008). Fibrosarcoma adjacent to the site of microchip implantation in a cat. J Feline Med Surg 10: 202-205
5. Wilcock B et al (2012) Feline postvaccinal sarcoma: 20 years later. Can Vet J 53: 430-434.
6. Couto SS,et al (2002). Feline Vaccine-associated Fibrosarcoma: Morphologic Distinctions. Vet Pathol 39:33–41.
7. Roesner A et al (2008) Oxidative stress in ulcerative colitis-induced carcinogenesis. Pathol Res Pract 204: 511-524.
8. Morrison BW, Starr RM, Vaccine-Associated Feline Sarcoma Task Force (2001).Vaccine-associated feline sarcomas. J Am Vet Med Assoc 218: 697-702 .
9. Davidson EB et al. (1997) Surgical Excision of Soft Tissue Fibrosarcomas in Cats. Vet. Surgery 26: 265-269.
10.Hershey AE, et al. (2000) Prognosis for presumed feline vaccine-associated sarcoma after excision: 61 cases (1986-1996). J Am Vet Med Assoc 216: 58-61.
11.Cronin K, et al (1998). Radiation therapy and surgery for fibrosarcoma in 33 cats. Vet Radiol Ultrasound, 39: 51-56
12. Bregazzi VS, et al (2001) Treatment with a combination of doxorubicin, surgery, and radiation versus surgery and radiation alone for cats with vaccine-associated sarcomas: 25 cases (1995-2000). J Am Vet Med 218: 547-550.
13.Cohen M, et al. (2001). Use of surgery and electron beam irradiation, with or without chemotherapy, for treatment of vaccine-associated sarcomas in cats: 78 cases (1996–2000) J Am Vet Med Assoc 219: 1582-1589.
14. Jas D, et al (2015) Adjuvant immunotherapy of feline injection-site sarcomas with the recombinant canarypox virus expressing feline interleukine-2 evaluated in a controlled monocentric clinical trial when used in association with surgery and brachytherapy. Trials in Vaccinology 4: 1-8
15. Vaccine-Associated Feline Sarcoma Task Force (2005) Round Table Discussion. The current understanding and management of vaccine-associated sarcomas in cats. J Am Vet Med Assoc 226: 1821-1842.

